原子がイオンになるときに出入りする電子の数 基本的に価電子の数によって決まる。 よって、周期表の族で価数がわかる。 4.覚えとくべきイオン 1~20番のイオンは、1族,2族 16族,17族,アルミニウムを覚えましょう。 今回は以上になります。. 次に銅(Cu)でみてみましょう。銅は陽イオンになりやすい性質があります。なので、持っている電子を失って陽イオンになろうとします。 ここで注意したいのは電子の数です。水素の場合は、陽子1コに対し電子が1コでしたが、銅は陽子を2コ、そして電子を2コ持っています。
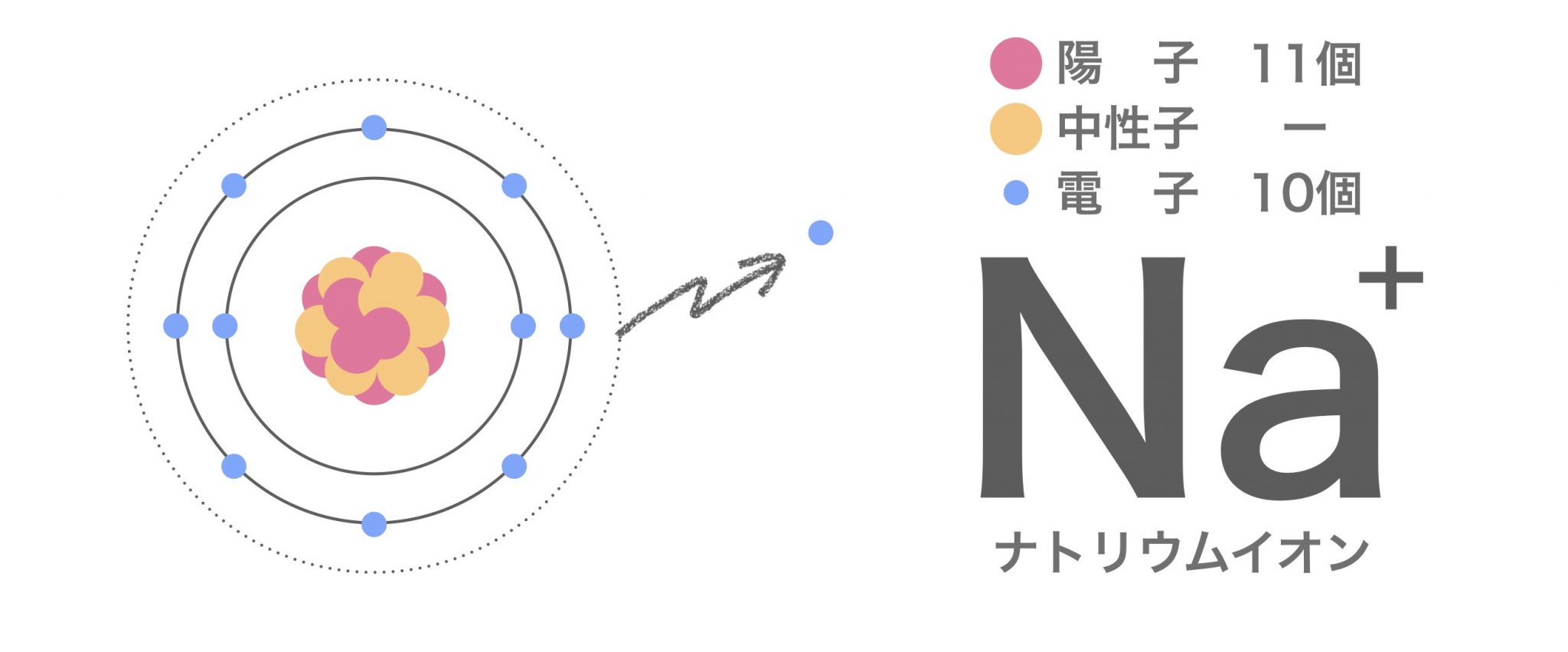
イオンと原子の違いは?覚えるべきポイントを徹底解説!|高校化学をスキマ時間でわかりやすく
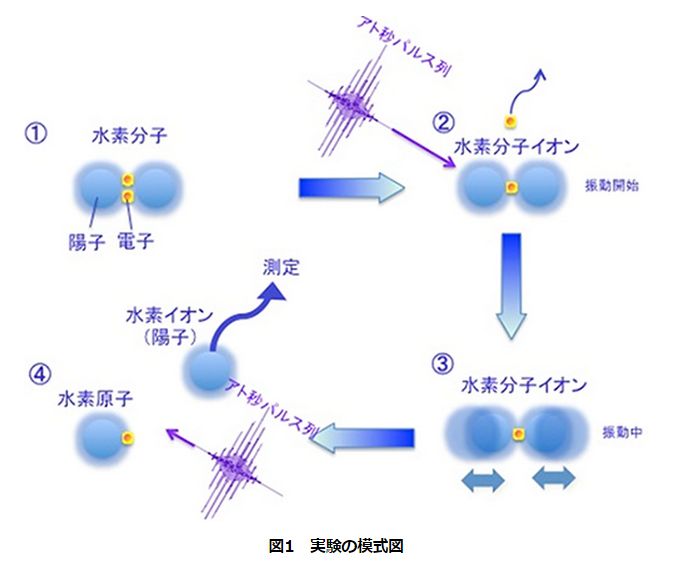
水素分子のイオン化は振動まで1000兆分の1秒:分子運動で新たな光の高速制御を?(1/2 ページ) EE Times Japan
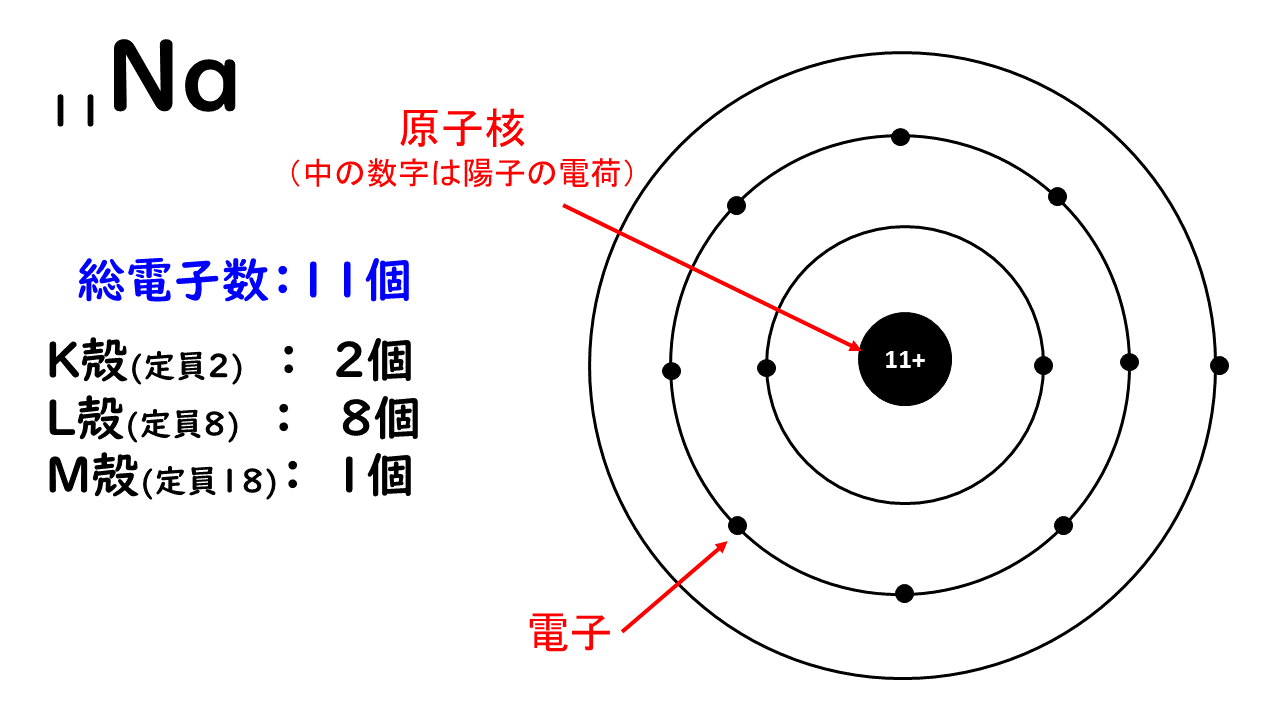
14. 電子殻と電子配置|おのれー|note
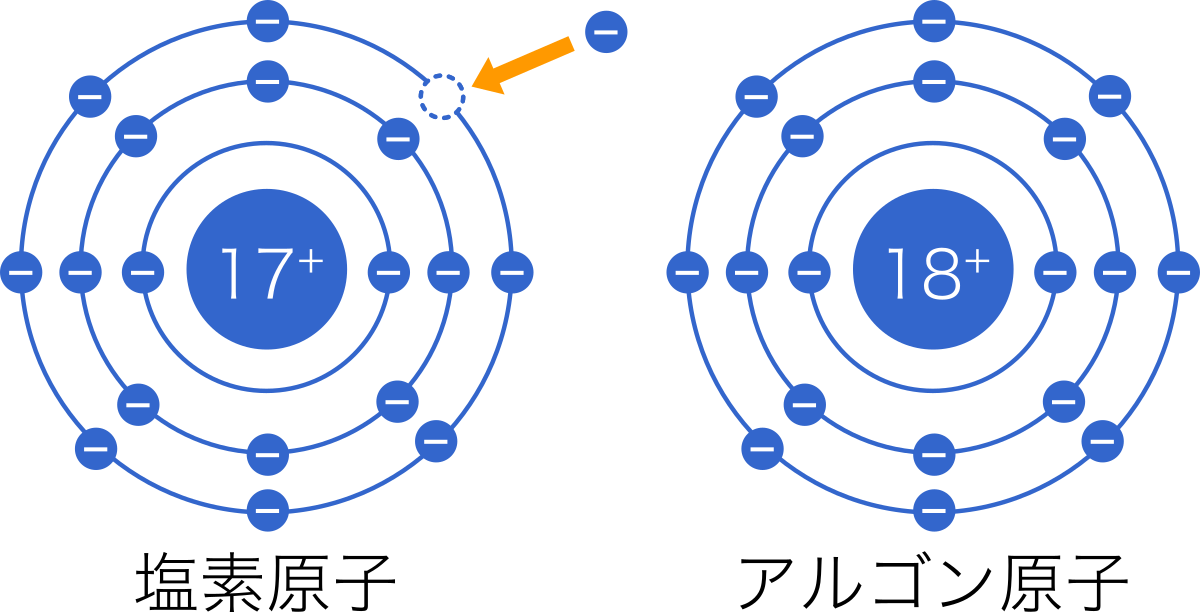
【高校化学基礎まとめ】イオン mm参考書
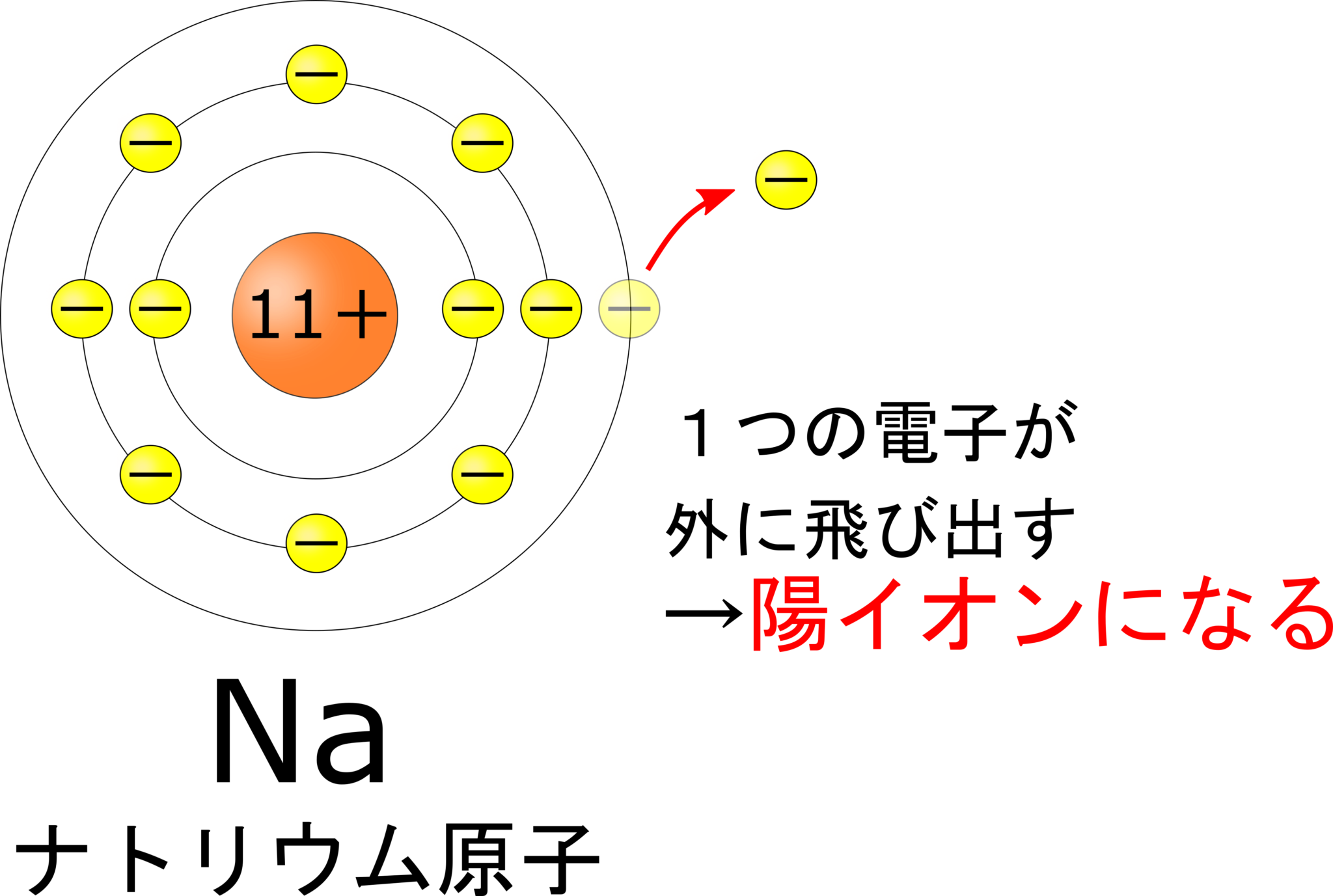
【中学3年】原子の構造を理解すればイオンが完璧に理解できる!【原子とイオンの関係とは!?】 理科の授業をふりかえる

【高校化学基礎】「電子式とは」 映像授業のTry IT (トライイット)

イオン化エネルギー徹底解説!周期表での法則も解説 │ 受験スタイル
![[4つ覚えるだけ] 電子配置の書き方 ゼロからの化学基礎 [4つ覚えるだけ] 電子配置の書き方 ゼロからの化学基礎](https://cdn-ak.f.st-hatena.com/images/fotolife/k/kemisupea/20220821/20220821143816.jpg)
[4つ覚えるだけ] 電子配置の書き方 ゼロからの化学基礎

3分で簡単にわかる「オクテット則」価電子のルールを理系ライターがわかりやすく解説 ページ 3 StudyZ
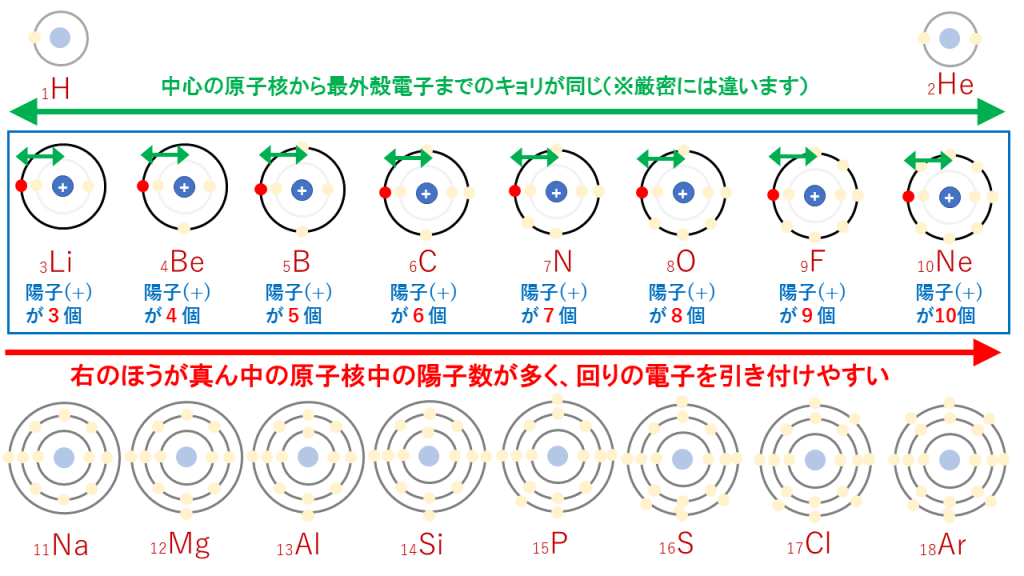
化学【5分でわかる】イオン化エネルギーの定義と大小関係とその理由 ViCOLLA Magazine
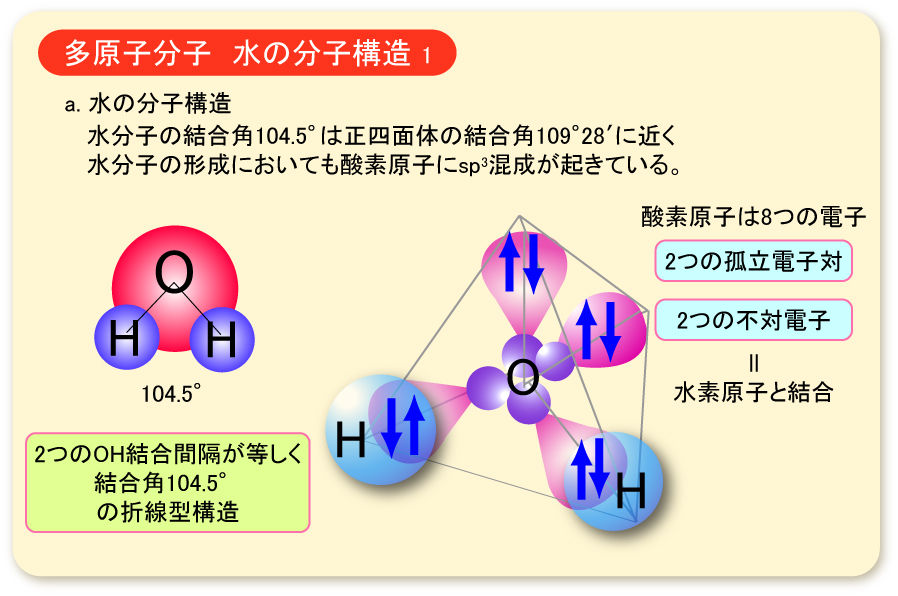
分子の形状 ねこでもわかる化学

価電子とは?数え方や覚え方 最外殻電子との違いは?
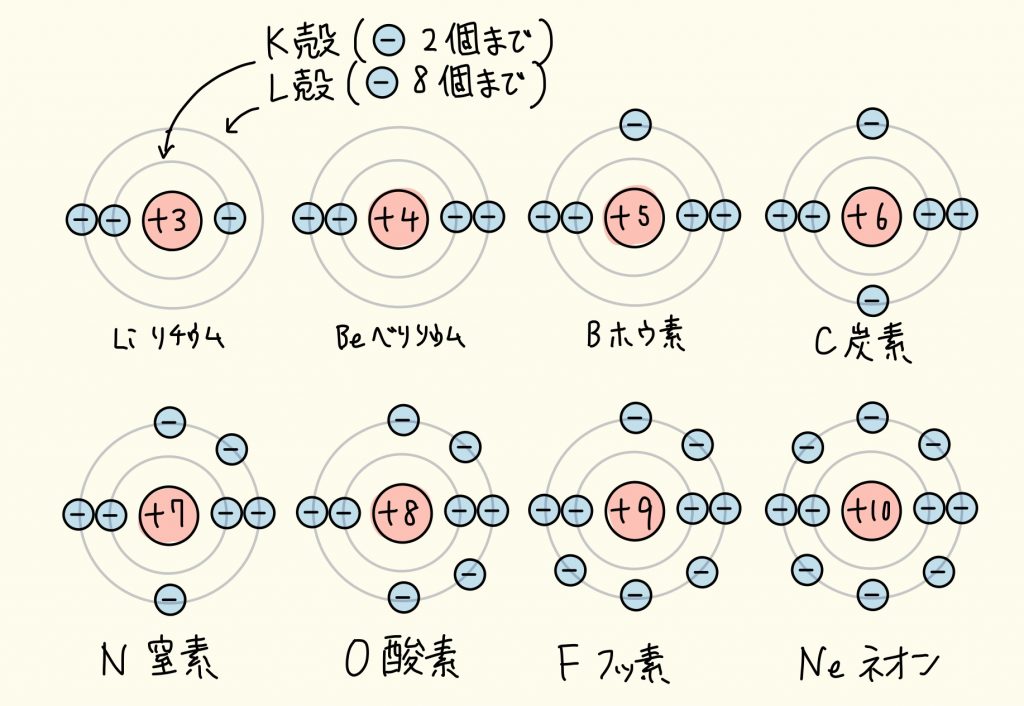
初歩!「原子の構造」をゆっくりていねいに解説するよ!【授業 レベルA2】 ともよし塾|無料授業・オリジナル問題
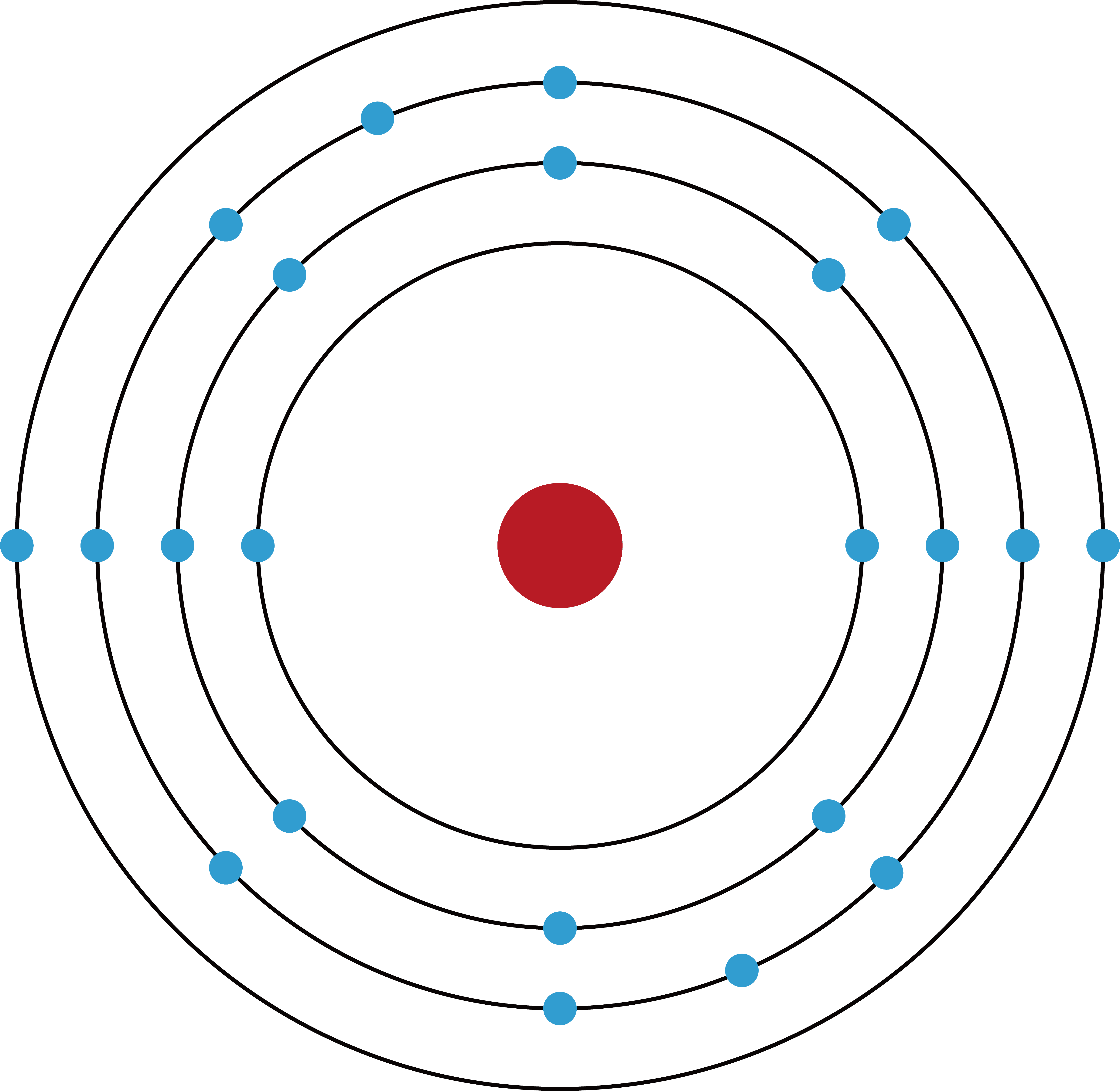
【図解】電子配置とは?例題で電子を並べる順番やルール、覚え方を解説! 化学のグルメ
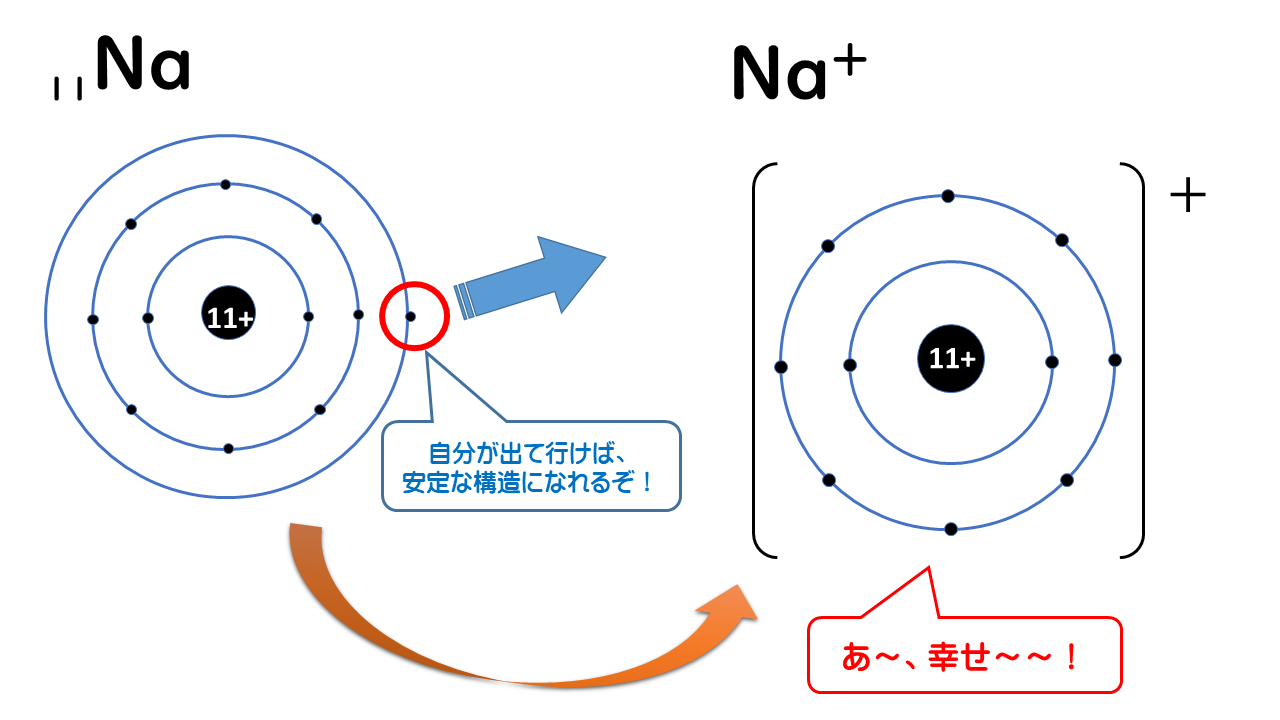
15. イオンの生成|おのれー|note
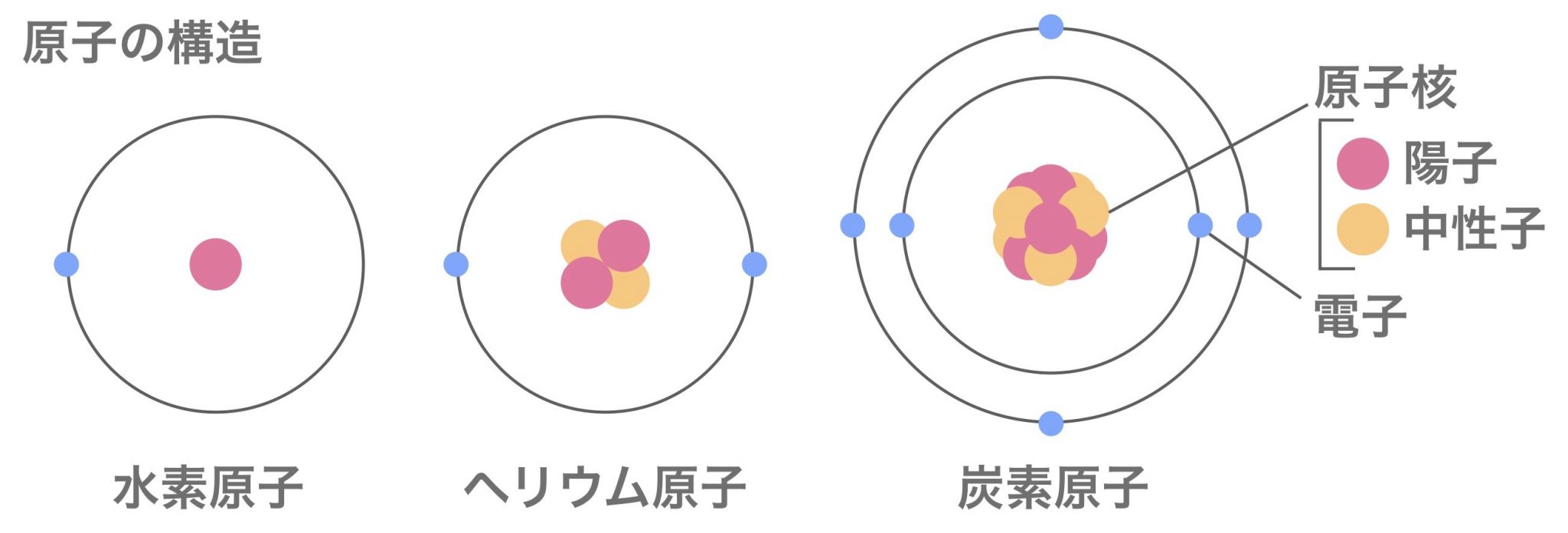
世界は3種類の粒からできている?原子の構造について。|高校化学をスキマ時間でわかりやすく
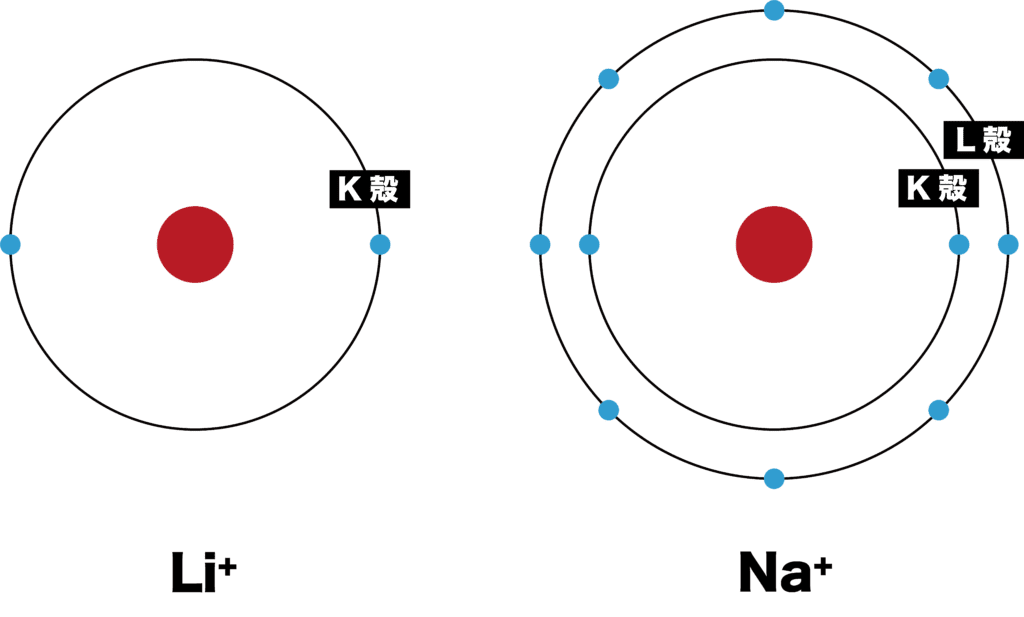
イオンの大きさ(原子の場合と異なる理由・周期表での傾向など) 化学のグルメ

【化学】イオンとは 分かりやすく解説 ゼロからの化学基礎
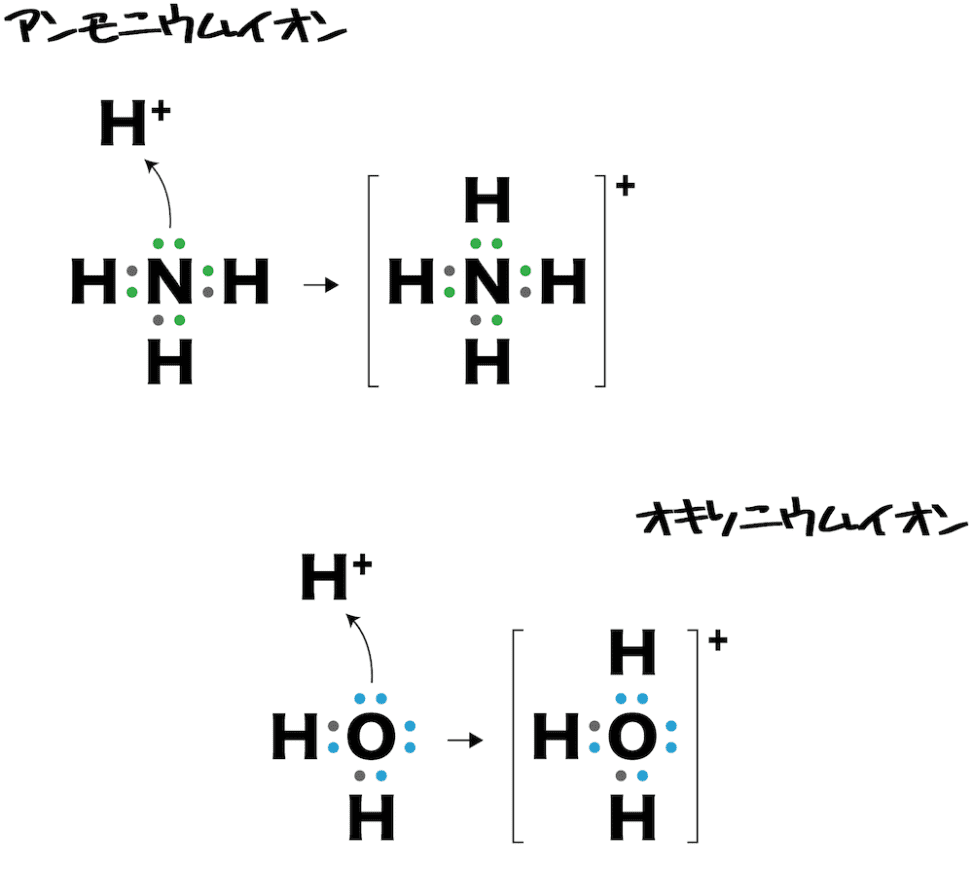
配位結合・錯イオン【高校化学・化学基礎一問一答】 化学のグルメ

原子価とは?原子価の求め方までわかりやすく解説|高校生向け受験応援メディア「受験のミカタ」
水素原子には電子が1個だけ含まれていますから、「水素様原子」にも水素原子と同じ数、つまり1個の電子が含まれています。. 今回は電子を1つしか持たない原子である「水素様原子」の電子についてのシュレディンガー方程式を立式しました。. 原子・イオン :質量数=陽子数+中性子数. 水酸化物イオンoh - の電子の総数. 水酸化物イオンを構成する原子oとhの電子の数をまず数えます。酸素原子oは原子番号8番ですので陽子の数が8個。したがって電子の数も8個。