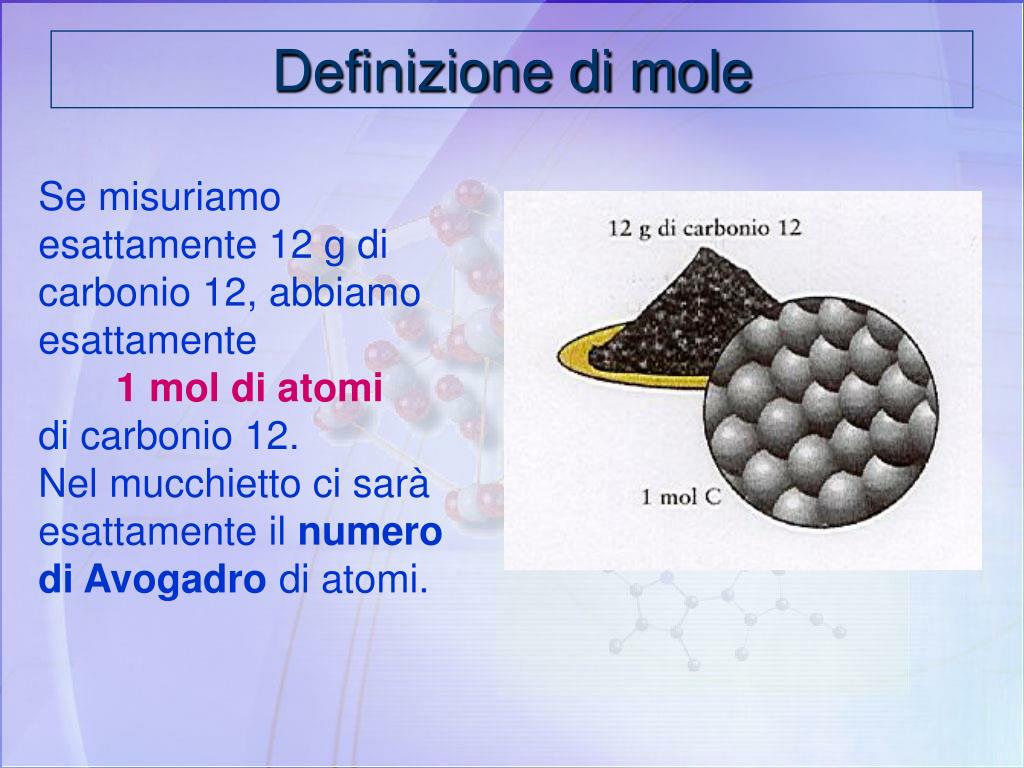
Cos'è il numero di moli e cosa rappresenta. Richiamiamo brevemente la definizione di mole.Diciamo che una mole (1 mol) di sostanza è la quantità di tale sostanza contenente tante entità fondamentali (atomi o molecole, a seconda dei casi) quante sono le entità fondamentali contenute in 12 grammi di isotopi 12 C del carbonio.. La mole è quindi una grandezza che misura la quantità di.. La costante di Avogadro, chiamata così in onore di Amedeo Avogadro e denotata dal simbolo o , è il numero di particelle costituenti (come atomi, molecole, ioni, elettroni o entità molecolari in generale) contenute in una mole di sostanza. Tale costante ha le dimensioni dell'inverso di una quantità di sostanza (cioè mol −1).Tale costante è pari a 6,02214076 × 10 23 mol −1.

PPT CORSO INTEGRATO DI BIOLOGIA, FISICA E CHIMICA a.a .201 02011 Dott.ssa Alessandra

PPT Molecole e moli PowerPoint Presentation, free download ID4580998

LEZIONE DI SCIENZE ATOMI E MOLECOLE in un... Mind Map

PPT Moli e numero di Avogadro PowerPoint Presentation, free download ID7064829

Introduzione alla chimica atomi, molecole, elementi e composti YouTube

"Esercizi Numero di Molecole" Chimica Generale YouTube
Chimica la tavola periodica degli elementi

PPT La Mole E Il Numero di Avogadro PowerPoint Presentation, free download ID4611024

PPT Chimica e laboratorio PowerPoint Presentation, free download ID524981

MOLE E NUMERO DI AVOGADRO Microlearning
PPT Lezione chimica 3 PowerPoint Presentation, free download ID5804731

PPT Calcoli applicati alla chimica analitica PowerPoint Presentation ID4086138

"Numero di Molecole" L45 Chimica Generale ManueleAtzeni ISCRIVITI YouTube

MOLE E NUMERO DI AVOGADRO YouTube

PPT Mole e Numero di Avogadro PowerPoint Presentation ID4354110
PPT “La Mole” Principi di stechiometria PowerPoint Presentation, free download ID4354029
PPT Molecole e moli PowerPoint Presentation, free download ID4580998
Numero Di Molecole In Una Mole beyarules

PPT “La Mole” Principi di stechiometria PowerPoint Presentation, free download ID4354029

PPT “La Mole” Principi di stechiometria PowerPoint Presentation, free download ID4354029
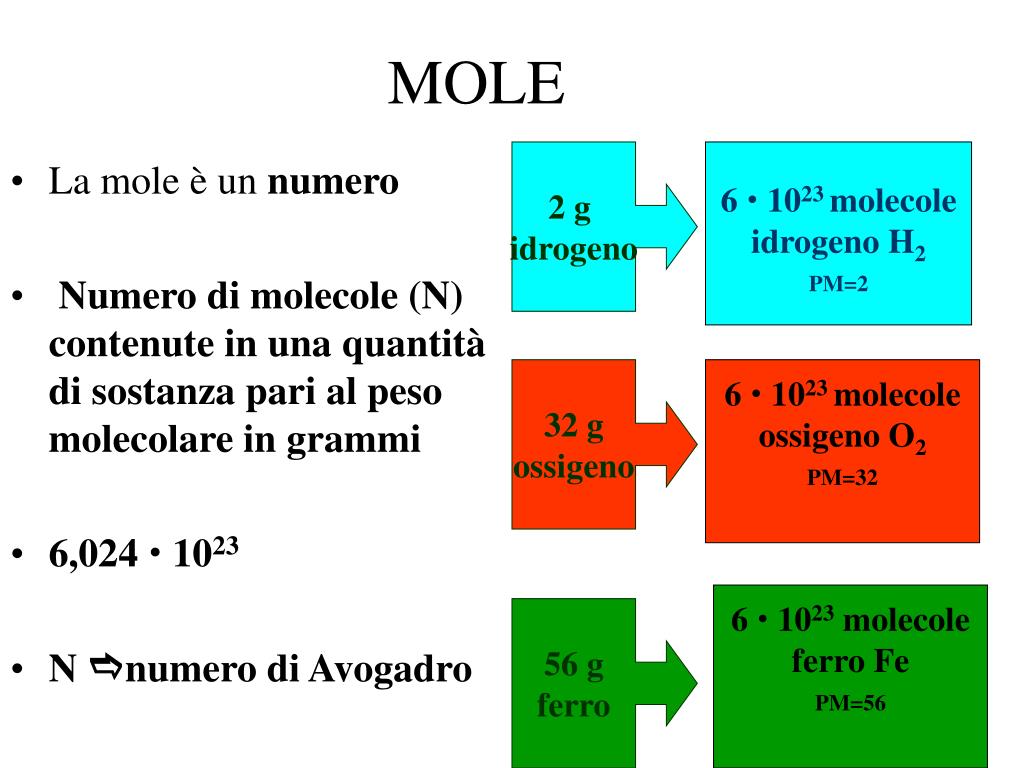
Il numero di Avogadro è una costante fisica che deriva dall'omonima legge di Avogadro, e che esprime il numero di entità fondamentali (atomi o molecole) contenute in 1 mole di sostanza. In modo equivalente, è il numero di atomi di carbonio 12 presenti in 12 grammi di tale sostanza. Eccoci giunti alla seconda, fondamentale nozione su cui si.. Quindi: una mole di idrogeno (H 2) contiene sempre 6,022·10 23 molecole. Il numero di Avogadro (N 0) rappresenta quindi il numero di entità contenute nella unità mole. Esso è un numero gigantesco: per cercare di capire quanto grande sia il valore di N 0 si consideri che una mole di chicchi di riso corrisponde a circa 20 milioni di miliardi.